 La tecnología de las baterías de litio-ion ha evolucionado significativamente, ofreciendo mayor estabilidad y eficiencia en productos cotidianos. Descubre cómo funcionan en PHEV y otros dispositivos electrónicos.
La tecnología de las baterías de litio-ion ha evolucionado significativamente, ofreciendo mayor estabilidad y eficiencia en productos cotidianos. Descubre cómo funcionan en PHEV y otros dispositivos electrónicos.
Las baterías de iones de litio son omnipresentes en laptops, smartphones, PDA y reproductores de música. Su popularidad radica en su alta densidad energética: libra por libra, superan a la mayoría de las baterías recargables disponibles.
Sin embargo, han ganado notoriedad por incidentes raros de ignición. Aunque solo afectan a 2-3 paquetes por millón, estos fallos extremos han provocado retiros masivos costosos para los fabricantes.
¿Cuál es el secreto de su potencia? ¿Por qué pueden incendiarse? ¿Cómo extender su vida útil? En este artículo experto, respondemos estas dudas con base en principios químicos y recomendaciones prácticas.
Ventajas clave sobre otras tecnologías:
- Alta densidad energética.
- Baja autodescarga (5% mensual).
- Sin efecto memoria.
- Mayor vida útil (500-1000 ciclos).
- Peso ligero y diseño compacto.
Desventajas notables:
- Riesgo de sobrecalentamiento e ignición.
- Sensibles a altas temperaturas.
- Degradación gradual desde la fabricación.
- Costo elevado.
Estas características se explican por su química interna. Exploremos una celda de litio-ion.
Dentro de una Batería de Iones de Litio

Los paquetes varían en forma, pero internamente son similares. No desarmes una batería: riesgo de cortocircuito e incendio. Encontrarás:
- Células individuales conectadas en serie/paralelo.
- Circuito de protección (PCB) que monitorea voltaje, temperatura y ciclos.
La Célula de Iones de Litio
Carcasa metálica presurizada con orificio de ventilación y PTC (coeficiente de temperatura positivo) para seguridad.
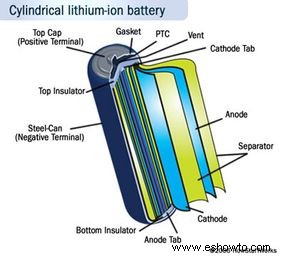
Contiene una espiral de tres láminas:
- Ánodo (negativo): Grafito con carbono.
- Cátodo (positivo): Óxido de litio-cobalto (LiCoO2).
- Separador: Plástico microperforado.
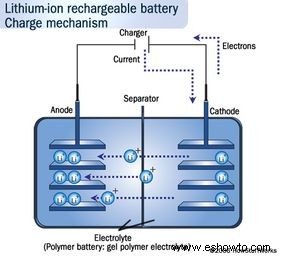
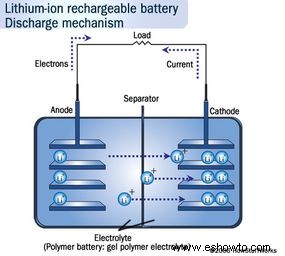
Esto permite diseños compactos. Más detalles en Cómo funcionan las baterías.
Vida Útil y Seguridad de las Baterías de Iones de Litio

Informes recientes destacan incendios en laptops por baterías defectuosas.
Para maximizar duración:
- Evita temperaturas extremas (ideal: 15-25°C).
- Carga al 80-90% habitual; evita 100% constante.
- No descargues por completo frecuentemente.
- Almacena al 50% en fresco si no usas.
- Actualiza firmware de dispositivos.
Baterías Explosivas: Causas
Incendios inician por sobrecalentamiento del electrolito. Cortocircuito interno (perforación del separador) genera calor extremo, libera electrolito inflamable y propaga fuego entre celdas.
Raros, pero mediáticos. Ejemplos en CBC: "Summer of the Exploding Laptop".
Publicado originalmente: 14 de noviembre de 2006. Actualizado con datos recientes.

