 ¿Cómo alimentan las baterías nuestro mundo? Explora imágenes detalladas de baterías.
¿Cómo alimentan las baterías nuestro mundo? Explora imágenes detalladas de baterías. Imagina un mundo donde todos los dispositivos eléctricos debieran estar enchufados permanentemente. Linternas, auriculares, teléfonos móviles y gadgets portátiles resultarían incómodos y poco prácticos. Los autos requerirían un arranque manual extenuante. Cables por doquier generarían riesgos y desorden. Afortunadamente, las baterías proporcionan energía móvil, haciendo posible la comodidad moderna.
Existen diversos tipos de baterías, pero su principio básico es idéntico: al conectar un dispositivo, se genera una reacción electroquímica que produce electricidad. El físico italiano Alessandro Volta descubrió este proceso en 1799 con su pila simple de placas metálicas y cartón empapado en salmuera. Desde entonces, los avances han creado baterías variadas en materiales y tamaños.
Hoy, las baterías están en todas partes: alimentan relojes por meses, mantienen teléfonos y despertadores durante cortes de luz, impulsan detectores de humo, maquinillas eléctricas, taladros, reproductores MP3 y más. Si lees esto en un portátil o smartphone, ¡estás usando baterías ahora mismo! Este artículo profundiza en su historia, partes, reacciones y procesos para apreciar mejor estas fuentes portátiles de energía.
Historia de las Baterías
 La historia de las baterías se remonta a 1800. Conoce su evolución y la construcción de la celda Daniell.
La historia de las baterías se remonta a 1800. Conoce su evolución y la construcción de la celda Daniell. Las baterías son más antiguas de lo que crees. En 1938, el arqueólogo Wilhelm König halló vasijas de barro en Khujut Rabu, cerca de Bagdad (Irak), de unos 5 pulgadas (12,7 cm), con barra de hierro recubierta de cobre, datadas en 200 a.C. Probablemente contenían ácido como vinagre, sugiriendo uso como baterías para rituales, medicina o galvanoplastia. Réplicas confirman que generan carga.
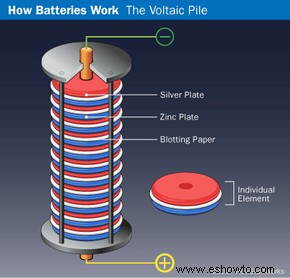
En 1799, Alessandro Volta inventó la pila voltaica: capas alternas de zinc, cartón empapado en salmuera y plata. Producía corriente constante, aunque limitada por peso y corrosión. Honra su legado la unidad de voltio.
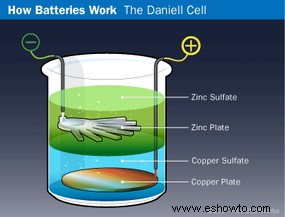
En 1836, John Frederick Daniell creó la celda Daniell: placa de cobre en frasco con sulfato de cobre, zinc suspendido en sulfato de zinc. Funcionaba para aplicaciones fijas como timbres y teléfonos pre-eléctricos.
En 1898, la Columbia Dry Cell fue la primera batería seca comercial en EE.UU., precursora de Energizer.
Continúa para conocer las partes de una batería.
Anatomía de una Batería
Cualquier batería tiene dos terminales: positivo (+) y negativo (-). En pilas AA, C o D, están en extremos; en autos o 9V, lado a lado. Conectar cables directamente causa cortocircuito peligroso. Para uso correcto, conecta a una carga como bombilla o motor.
En su carcasa de metal o plástico hay un cátodo (positivo), ánodo (negativo), ambos electrodos donde ocurren reacciones. Un separador los aísla, permitiendo flujo eléctrico. El electrolito conduce iones entre ellos. El colector lleva la corriente externa.
Siguiente: cómo generan corriente.
Reacciones y Química de las Baterías
Al insertar una batería, reacciones electroquímicas generan electricidad. El ánodo sufre oxidación: iones del electrolito liberan electrones. El cátodo, reducción: absorbe electrones. Resultado: flujo de electrones (electricidad) hasta agotar reactivos.
Químicas comunes: zinc-carbono, alcalinas, NiCd, NiMH, Li-ion, plomo-ácido.
Experimentos con Pilas: Replica la Pila Voltaica
Construye tu pila: multímetro ($10-20), monedas de 25¢, aluminio, papel secante, vinagre de sidra y sal. Apila: aluminio (ánodo), papel salino (separador/electrolito), moneda (cátodo). 10 repeticiones encienden un LED.
O usa limón: alambre cobre, clip, exprime limón, inserta sin tocar. Mide voltaje/corriente.
Baterías Recargables
Desde 1859 (Gaston Planté, plomo-ácido), las recargables revierten reacciones aplicando corriente externa. Comunes: Li-ion (alta capacidad, sin memoria), NiMH, NiCd (efecto memoria).
Li-ion evitan sobrecarga, no necesitan reacondicionamiento. Recicla al final.
Disposición y Alimentación de Baterías
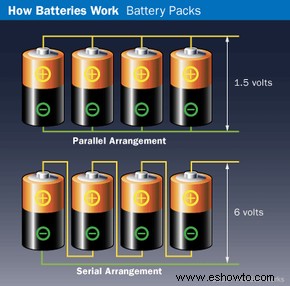
Serie: suma voltajes (ej. 4x1,5V=6V). Paralelo: suma corriente (4x500mAh=2000mAh).
La tecnología avanza hacia baterías más eficientes para nuestro mundo portátil.
Preguntas Frecuentes sobre Baterías
¿Qué es la energía de una batería?
Vatios-hora (Wh): voltaje (V) x amperios x horas.
¿Cuáles son los tipos de baterías?
Zinc-carbono, alcalinas, Li-ion (recargables), plomo-ácido, aire-litio en desarrollo.
¿Cuánto cuesta una batería de coche?
$50-120 típica; $90-200+ con garantía extendida.
¿Cuál es la fuente de energía?
Reacción electroquímica: oxidación en ánodo crea electrones; reducción en cátodo los absorbe.
¿Tipos de recargables?
Li-ion, NiMH, NiCd.
Publicado originalmente: 1 de abril de 2000

